Sarkoidose - Faglige retningslinjer for sarkoidose
Patologisk og cytologisk diagnostikk
Sist faglig oppdatert: 15.05.2022
Göran Elmberger
Innledning
Sarkoidose er en systemsykdom karakterisert av ikke nekrotiserende granulomer i ulike organer. Lesjonenes distribusjon taler for at lungene utgjør introduksjonsvei for det formodede eksogene agens som forårsaker sykdommen. Deretter synes det å skje en spredning til de mediastinale lymfeknutene via lymfen. Øvrige organer rammes deretter ved en kombinasjon av lymfogen og hematogen spredning. Utviklingen ligner den vi ser ved tuberkulose.
Histopatologisk og cytologisk bilde
Generelt baseres diagnostikken på funn av ikke nekrotiserende granulomatøs inflammasjon i de affiserte vevene. Granulomet, som er karakteristisk for sarkoidose, utgjøres av en skarpt avgrenset, kompakt, ballformet opphopning av epiteloidceller med innslag av multinukleære kjempeceller, oftest av Langerhansk type (Figur 1 a, b). Epiteloidcellen er en cytoplasmarik, høyt differensiert mononukleær histiocyt (Figur 2 a-d). Den oppviser ultrastrukturelt en transformasjon fra fagocyterende til sekretorisk fenotype. De flerkjernede kjempecellene kan inneholde cytoplasmatiske inklusjoner som asteroidelegemer, forkalkede Schaumannlegemer, eller dobbeltbrytende endogene krystaller av kalsiumoksalat- eller kalsiumkarbonat-type. Slike krystaller kan for patologen være vanskelig å skille fra eksogent materiale, derfor risikerer han å oppfatte dem som materiale fra fremmedlegemer. Ved immunhistokjemisk fargning ses i epiteloidcellene cytoplasmatisk forekomst av angiotensin converting enzyme (ACE), men det er ikke spesifikt for epiteloidcellegranulomer. Andelen lymfocytter som deltar i granulomdannelsen er i det typiske tilfellet lavt, men sannsynligvis forekommer en betydelig tidsmessig variasjon i løpet av granulomet utvikling. Initialt forekommer mest CD4+ T- hjelperlymfocytter. Disse antas å bidra til dannelsen av granulomer ved å attrahere histiocytter og understøtte transformasjonen til epiteloidceller. I det modne granulomet forekommer i stedet for det meste CD8+ T- celler. CD4+- cellene tenderer å lokaliseres mer sentralt i granulomene enn - CD8+ cellene. I opp til en tredjedel av tilfellene ses en fokal koagulativ nekrose med fibrinoiddeposisjon. I motsetning til den ostelignende nekrosen som ses ved tuberkulosegranulomer, forblir det imidlertid et intakt, diskré retikkelnettverk ved sarkoidose. Retikkelfargning, for eksempel etter Gordon-Sweet, kan derfor ha en viss differensialdiagnostisk verdi. Granulomene kan med tiden enten gjennomgå resolusjon, eller utvikle et fibroseinnslag, som initialt tar form som konsentriske kollegene lameller langs granulomenes periferi. Etter hvert kan fibrose progrediere sentralt, og i sluttstadiet gjenstår ofte kun et ballformet hyalinisert fibrotisk område, eventuelt med innslag av resterende Schaumann- legemer. I det enkelte tilfellet ses ofte granulomer av forskjellig modningsgrad- temporal heterogenisitet; dette antyder at den ikke identifiserte årsaksfaktoren er kontinuerlig aktiv.
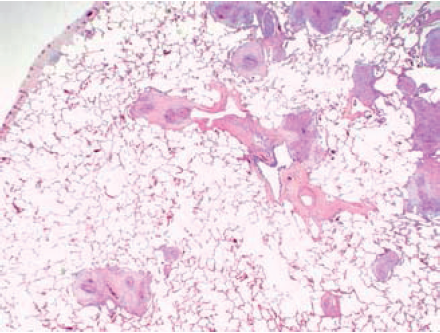
Figur 1. Histologiske bilder av sarkoidose i ulike organer
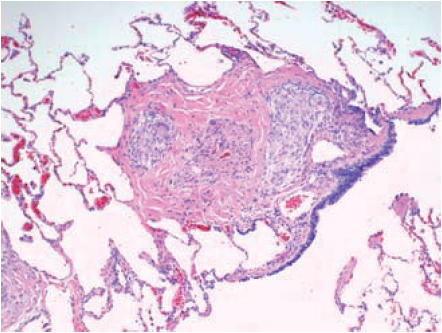
- Lunge. 32 årig kvinne med tørrhoste, tretthet, anstrengelsesdyspné og leddsmerter i cirka ett år. Bilaterale lungeinfiltrater, overveiende i de apikale underlappene. Kile-eksisjon fra underlapp. Mikroskopisk ses rikelig med epiteloidcellegranulomer. Utpreget lymfangittisk distribusjon med engasjement av pleura, peribronkiolære sentrilobulære strukturer og septa i lobulis periferi. (Htx; X 2)
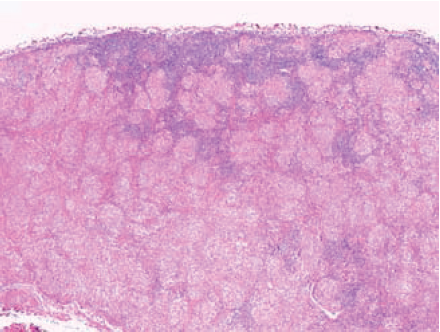
- Lymfkeknute. Tidligere frisk 17 årig mann som ble syk tre måneder tidligere, med lymfeknutehevelser på halsen og ved bøyefuren på albuene. Videre bilaterale lungeinfiltrater. Lymfeknute ekstirpert fra halsen viser rikelig med små diskré ballformede granulomer av jevn størrelse. Ingen nekrose. Et visst fibroseinnslag. Lungebiopsi senere viser også granulomforekomst. (Htx; X 4)
(Samtlige bilder i kapittelet er hentet fra Selroos O, Eklund A. Sarkoidos. Studentlitteratur, Lund 2008.)
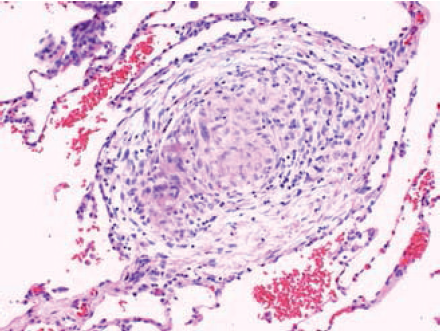
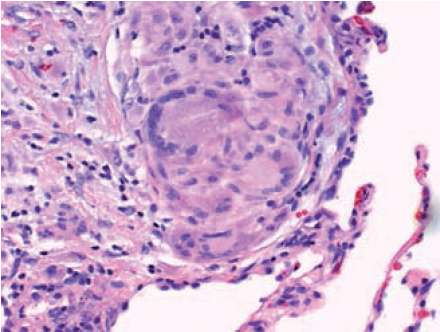
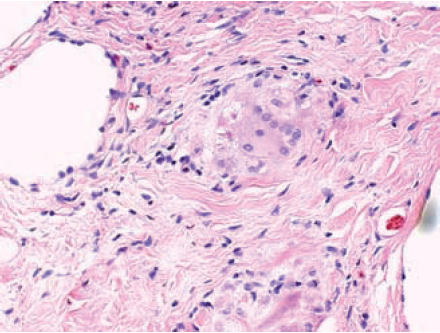
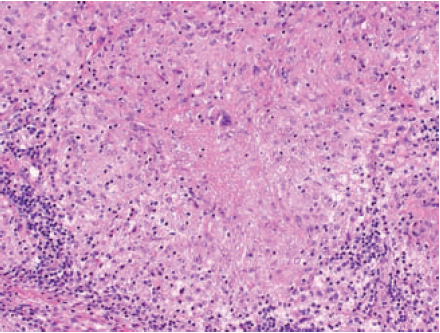
Figur 2. Sarkoidosegranulomer i stor forstørrelse
- Oversikt. Interstitielt ikke nekrotiserende granulomer i lunge.Sentralt ses epiteloidceller omgitt av løsmaskede lymfocyttære infiltrater. Diskré løsmasket fibrose i granulomets periferi. (Htx; X 20)
- Epiteloidcellegranulom med konglomerat av Langhanske kjempeceller. Kjempecellene oppviser syncytialt cytoplasma med omtrent 20 monomorfe kjerner anordnet i en perifer hestesko- lignende formasjon. (Htx; X 40)
- Langerhansk kjempecelle med to asteroidelegemer (Htx; X 40)
- Fibrinoid nekrose ses sentralt i dette lymfeknutegranulomet. (Htx; X 20)
Faktarute 1. Histopatologiske karakteristika ved lungsarkoidose
Viktige positive funn Ikke-nekrotiserende granulomer Velavgrensede, tett liggende, eventuelt hyaliniserte Lymfangittisk distribusjon Øvrige positive funn Vaskulitt i 1/3 av de åpne lungebiopsiene Punktformet fibrinoid nekrose i 1/3 av de åpne lungbiopsiene Inklusjonslegemer Schaumannlegemer Asteroidelegemer Dobbeltbrytende krystaller (kalsiumkarbonat eller -oksalat) Mikroforkalkninger Hamazaki-Wesenberglegemer Viktige negative funn Fravær av mikroorganismer ved spesialfargning og dyrkning Ingen eksposisjon for mineralstøv (beryllium, talkum, aluminium) Kun lett kronisk interstitiell inflammasjon Komplikasjoner Interstitiell reorganiserende fibrose av bikakenatur Kavernedannelse med saprofytisk vekst av Aspergillus |
Respirasjonsorganene
Sarkoidose rammer sjelden slimhinnene sinonasalt, men kan i enkelte tilfeller forårsake erosjon av ben og luftveisobstruksjon Det er rapportert subglottisk stenose og larynxpolypper. Ved lungeengasjement finnes ofte granulomer med såkalt lymfangitisk distribusjon (Faktarute 1). Dette innebærer at de fleste granulomene ses i tilknytning til større bronkier, i nærheten av bronkioli, subplevralt eller perivenulært i interlobulære septa. Ved nodulær sarkoidose, som forekommer i 5% av tilfellene, preges bildet av større, makroskopisk synlige områder med konfluerende granulomer, med relativt normalt lungeparenkym imellom. I en del tilfeller foreligger endobronkial sarkoidose med risiko for utvikling av obstruktivitet. Med unntak av i svært tidlig fase av sykdommen, er interstitiell, uspesifikk inflammasjon ikke noe fremtredende trekk ved sarkoidose.
I lungebiopsier som er tatt ved åpen kirurgi eller ved videoassistert thorakoskopi (VATS) kan vaskulitt, delvis av granulomatøs karakter, påvises i en drøy tredjedel av tilfellene. Avansert vaskulitt er antatt å kunne lede til pulmonal hypertensjon og cor pulmonale. Vanligvis utgjør interstitiell fibrose ikke noe problem ved sarkoidose, men unntaksvis kan progressiv lungefibrose med utvikling av reorganiserende bikakemønster komplisere forløpet (Figur 3 a, b).
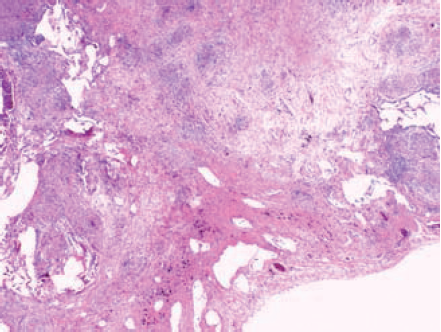
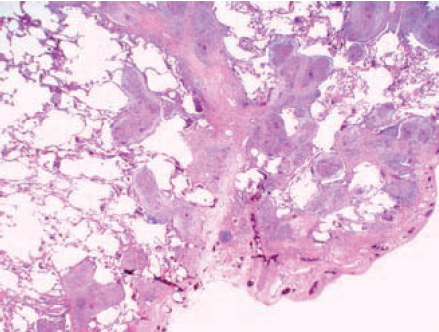
Figur 3 a, b. Histopatologisk bilde ved sarkoidose i lunge hos 33 år gammel mann med ankelartritt 6 måneder tidligere. Røntgen viser kraftig forstørrede mediastinale lymfeknuter og parenkyminfiltrat.
- Interstitiell fibrose kompliserer her bildet. Nærmest reorganiserende fibrose av ”honey-coombing” karakter. Granulomer består imidlertid fortsatt i bakgrunnen. (Htx; X 4)
- I andre områder er bildet ikke fullt så uttalt, men radiologisk påvisbare og makroskopisk synlige områder ses i flere deler av lungen. Snitt fra disse partier viser nærmest nodulær sarkoidose. (Htx; X 4)
Plevralt engasjement ved sarkoidose er svært uvanlig, men kan gi opphav til bilateral eksudasjon, chylothorax, pleurafortykkelse, forkalkning og «spontan» pneumothorax.
Lymfeknuter
Lymfeknutene er nesten alltid engasjert ved sarkoidose. De mest uttalte forandringene ses peribronkialt og mediastinalt. Blant de overflatiske stasjonene ses oftest engasjement på halsen, fossa supraclavicularis og i aksiller, men alle perifere lymfeknutestasjoner kan rammes. Lymfeknutene er som regel moderat forstørrede, (<20 mm), faste i konsistensen, og ofte ikke adherente, i motsetning til reaksjonen for eksempel ved tuberkulose.
Sarkoidose og kreft
Ved sarkoidose foreligger en økt risiko for at maligne tumores kan oppstå. Intervallet mellom sarkoidosediagnose og tumor er ikke sjelden omkring ti år. Dette faktum er det viktig at både klinikere og patologer kjenner til, slik at unødvendig «doctor’s delay» ved prøvetagning og vurdering ikke oppstår. I denne sammenhengen er det også viktig å nevne at en sarkoid reaksjon med epiteloidcellereaksjon ikke sjelden forekommer i direkte tilknytning til mange tumores og i de drenerende lymfeknutene. Noen ganger kan nodulær sarkoidose i lunge og andre organer simulere kreft såvel klinisk som radiologisk. Det foreligger altså en risiko for overdiagnostikk av sarkoidose og feildiagnose av malignitet.
Morfologisk diagnostikk av sarkoidose
Diagnosen sarkoidose kan ikke fastslås på grunnlag av det histologiske bildet alene. Funn av ikke nekrotiserende granulomer med typisk utseende i to eller flere organsystemer støtter konsensusdiagnose under forutsetning av at morfolo differensialdiagnoser kan utelukkes (Faktarute 2).
Faktarute 2.
| Lunge | Lymfekjertler | Øvrige organer |
| Tuberkulose | Tuberkulose | Tuberkulose |
| Atypisk mykobakteriose | Atypisk mykobakteriose | Brucellose |
| Soppinfeksjon | Toksoplasmose | Øvrige infeksjoner |
| Eksogen alveolit | Kikuchis sykdom (benign subakutt nekrotiserende lymfadenitt) | Morbus Crohn |
| Pneumokoniose (berylliose) | Cat-scratch disease | Kjempecellemyokarditt |
| Legemiddelreaksjon | Hodgkins lymfom | GLUS |
| Aspiration | Non-Hodgkins lymfom | |
| Wegeners granulomatos | Langerhans cell histiocytosis | |
| Idiopatisk interstitiell pneumoni | GLUS (granulomatous lesions of unknown significance) |
Granulomatøse sykdommer med kjent etiologi og lokale sarkoide reaksjoner bør derfor først utelukkes (Faktarute 3). Sarkoidosegranulomene har riktignok et karakteristisk lysmikroskopisk utseende – diskré, velavgrensede, kjempecellerike, homogen størrelse, lymfocyttfattige, minimal fibrose, ikke-nekrotiserende - men bildet kan ikke sies å være spesifikt. Immunhistokjemiske eller andre spesialundersøkelser tillater ikke heller en positiv konklusjon angående granulomenes årsak, selv om ACE-positivitet og T-lymfocyttdominans kan gi en pekepinn (Figur 4; Faktarute 4). Infeksjon utgjør en spesielt vanlig differentialdiagnose mot sarkoidose. Derfor bør en morfologisk evaluering av et panel med histokjemiske og eventuelt immunhistokjemiske fargninger alltid utføres på vevsprøven, med tanke på å avsløre mikroorganismer av ulike typer (Faktarute 5). Det foreligger I dag visse muligheter til å utføre avansert mikrobiologisk molekylær diagnostikk på paraffinblokket materiale. Sarkoidose er imidlertid fra morfologisk synsvinkel en såkalt utelukkelsesdiagnose.
Faktarute 3. Sykdommer/tilstander med sarkoid vevsreaksjon
MaligniteterLymfom av Hodgkins og Non-Hodgkins type Lungecancer Karsinoid Blastcelletumorer Granularcelletumor Autoimmun systemsykdomSystemisk lupus erythematosus (SLE) Sjögrens syndrom Primær biliær cirrhose Familiær granulomatøs artritt Hiv infeksjonVaskulitsyndromWegeners granulomatose Disseminert visceral kjempecellearteriitt Systemisk nekrotiserende vaskulitt Takayasus arteritt Transplantasjon |
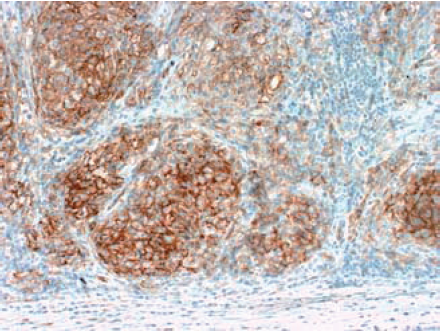
Faktaruta 4.
| Spesialfargninger for å etablere diagnose | |
| Vev/celletype | Fargning |
| Epiteloidcelle | CD68; ACE |
| T-lymfocytt | CD3; CD5 |
| T-helper celle | CD4 |
| T-suppressor celle | CD8 |
| B-lymfocytt | CD20; CD79a |
Faktaruta 5.
| Spesalfargninger for å utelukke infeksiøse organismer | |
| Mikroorganismer | Fargning |
| Bakterier | Gram |
| Mykobakterier | Putt |
| Sopp | Grocotte; PAS + diastas |
| Parasitter | Giemsa |
| Spirocheter | Warthin-Starry |
Lokalisasjoner som egner seg for biopsi
I første rekke biopseres slike vev eller organer der patologiske forandringer kan mistenkes ved klinisk eller radiologisk utredning. Dersom det foreligger forstørrede overfladiske lymfeknuter eller hudforandringer, er biopsier fra dem den enkleste måten å bekrefte granulomforekomst på. Tidligere utgjorde også biopsier av scalenuslymfeknutene (ad modum Daniel) et vanlig utredningsinnslag ved sarkoidose, men det er få som i dag er lært opp til å ta slike biopsier.
Bronkialslimhinnebiopsier og transbronkielle lungebiopsier (TBB) utgjør fremdeles, i kombinasjon med typisk klinikk og radiologi, et vanlig grunnlag for diagnose. TBB kan hos trenede skopister gi en sensitivitet > 90 %, dersom pasienten har sarkoi- dosetypiske radiologiske lungeinfiltrater. Dersom bilateral lymfeknuteforstørrelse foreligger alene, synker sensitiviteten markant til ~ 50 %. For å oppnå høy sensitivitet, kreves at biopsiene initialt snittes i nivåer, og at nedsnitting deretter utføres dersom ingen granulomer sees primært. Ultralydveiledning muliggjør punksjoner av mediastinale lymfeknuter via luftveiene (EBUS) eller øsofagus (EUS), som gir gode forut- setninger for å påvise granulomer. Det er ganske uvanlig at åpen lungebiopsi eller prøvetagning fra lungeparenkymet via videoassistert thorakoskopi (VATS) kreves for å bekrefte diagnosen sarkoidose. Mediastinalt forstørrede lymfeknuter kan også undersøkes ved at biopsi tas ved mediastinoskopi. Indikasjonen for mediastinoskopi øker dersom det er mistanke om malign genese, f.eks. dersom kliniske tegn på lymfom foreligger. Dersom man får tilstrekkelig utbytte ved prøvetagningen, er det tilrådelig at man også undersøker materialet med flowcytometrisk teknikk, for å påvise tegn på for eksempel klonal celle-ekspansjon.
Av og til kan man være nødt til å overveie slumpmessig biopsi fra organer som ikke oppviser tydelige forandringer, og ikke sjelden påvises da selv tidlig i sykdomsforløpet granulomer. Eksempel på organer som kan være aktuelle for blind biopsi er lever, milt, konjunktiva, tverrstripet muskulatur og benmarg. Sensitiviteten er sterkt varierende, men kan ligga i størrelsesorden 50- 60%.
Risikoen med blind biopsi av spesielt parenkymatøse indre organer gjør imidlertid at denne framgangsmåten for tiden er relativt uvanlig.
Det diagnostiske utbyttet ved biopsi er ikke alene avhengig av hvor biopsien er tatt, men også av sykdomsaktiviteten. Av avgjørende betydning for sensitiviteten er måten biopsien utføres teknisk. Det må tas tilstrekkelig mange biopsier av god størrelse, og materialet må ivaretas på en skånsom måte for å unngå artefakter. Ofte foreligger ikke noe åpenbart behov for analyse av ferskt materiale, og da anbefales formalinfiksering av biopsiene i 24 timer. På patologlaboratoriet bør biopsiene gjennomgå vanlig parafininnstøpning, og det bør gjøres forsiktige snitt for foreløpig vurdering om granulomer forekommer eller ikke. Ved granulomforekomst bør de videre diagnostiske tiltakene innrettes mot å påvise eventuelle infeksiøse agens. Dersom granulomer ikke kan påvises i de initiale snittnivåene, bør biopsiene deretter nedsnittes.
Man har framgangsrikt utført finnålsaspirasjon (FNA) ved ultralydsveiledet prøvetagning fra mediastinale lymfeknuter, som nevnt ovenfor, men også fra retroperitoneale, abdominale og intrapelvine lymfeknuter (Figur 5 a, b). Finnålspunksjon av milt, lever, spyttkjertler og selvsagt fra perifere lymfeknuter har også vært beskrevet ved morfologisk diagnostikk av sarkoidose. Metoden passer også godt når man ønsker å ivareta materiale for mikrobiologisk diagnostikk. En begrensning ved morfologisk analyse basert på FNA, er at sensitiviteten for en stor del er operatørsavhengig, og at det begrensade utbyttet sjelden tillater en adekvat framføring med vanlige infeksjonsfargninger.
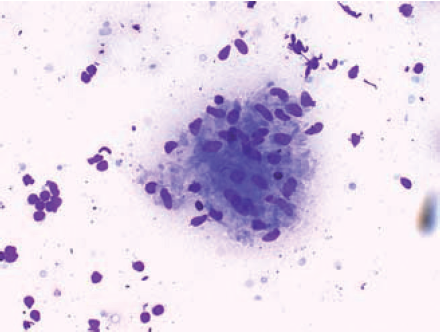
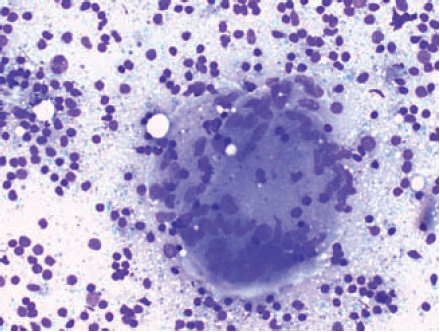
Figur 5 a, b. Cytologisk bilde ved sarkoidose. 34 årig kvinne med persisterande lymfadenopati i venstre fossa supraclavicularis. Finnålsaspiration viser ikke-nekrotiserande granulomatøs infeksjon.
- Fragmenter av epiteloidcellsgranulom. I bakgrunnen ses lymfocyter og enkelte røde blodceller. (Giemsa; X 40)
- Langhansk kjempecelle. Det cytologiska bildet gir nesten et 3-D intrykk der ett 50-talls kjerner ses i den syncytiella cytoplasman. (Giemsa; X 40)
Differensialdiagnostikk ved granulomatøs inflammasjon
Sarkoid reaksjon kan foreligge i de fleste vev, og kan derfor simulere sarkoidose uansett hvor biopsien tas (Figur 6; Faktarute 3). Differensialdiagnostikken for øvrig er ulik, delvis avhengig av hvilket organ som er engasjert (Faktarute 2).
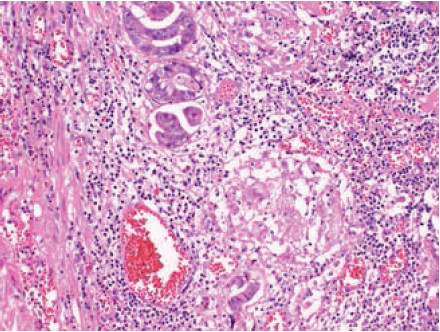
Til tross for adekvat utredning, kan en spesifikk diagnose av granulomatøs inflammasjon ikke stillas hos 15-20 % av tilfellene. Disse pasientenes sykdomsprosess kalles ofte GLUS syndrom (Granulomatous Lesions of Unknown Significance). Granulomene ved GLUS, toksoplasmose og de sarkoide vevsreaksjonene oppgis å inneholde B-lymfocytter, i motsetning till de T-lymfocytt- dominerte granulomene ved sarkoidose og tuberkulose.
Necrotizing sarcoid granulomatosis (NSG) er en tilstand som hovedsakelig manifesterer seg i lungene i form av konfluerende, nodulære grupperinger av sarkoidlignende epiteloidcellegranulomer. Granulomene ved NSG oppviser oftest ekstensiv nekrose og vaskulitt. Det er ennå omdiskutert om NSG utgjør en variant av sarkoidose, et vaskulittsyndrom eller et eksempel på nekrotiserende, inaktiv granulomatøs inflammasjon sekundært til et uidentifisert infeksiøst agens (Figur 7).
Hva som bør framgå av den patologisk-cytologiske uttalelsen (PAD)
Uttalelsen bør gi informasjon om biopsienes antall, størrelse, representativitet og sammensetning som tilbakemelding til prøvetageren. Frekvensen av granulomer, tilblanding av lymfocytter og fibrosegraden kan eventuelt være veiledende i aktivitetsvurderingen. Resultatene av gjennomførte immunhistokjemiske og histokjemiske spesialfarginger for granulomklassifikasjon og vurdering av eventuell forekomst av infeksjon bør dokumenteres.
Da sarkoidose jo er en morfologisk utelukkelsesdiagnose, kan diagnosen aldri entydig fastslås av patologen. Ved typisk morfologisk bilde og i fravær av støtte for mikrobiell eller annen differensialdiagnose, kan den patologiske uttalelsen for eksempel formuleres: «Ikke nekrotiserende granulomatøs inflammasjon der det morfologiske bildet kan passe godt med sarkoidose.»
Konsultasjon, konferansevirksomhet og konsensusdiagnostikk
Dersom den enkelte patologen har lite erfaring med sarkoidosediagnostikk, kan konsultasjonsvirksomhet innen spesialiteten være bra ved mer uvanlige sykdomsmanifestasjoner. Som ved all diagnostikk av ikke- neoplastisk lungesykdom, er samlede vurderinger ved konferanser av multidisiplinær type å anbefale. Sammenfatning av klinisk informasjon, BAL- data, radiologisk og morfologisk bilde gir forutsetninger for god konsensusdiagnostikk. Arbeidsmetodikken er også meget stimulerende og lærerik for alle deltagende nisjespesialister.
Referanser
- Fabian E, Vezendi S, Kormos M, Kiss I. Cytological investigation of biopsy performed in sarcoidosis. Z Erkr Atmungsorgane 1977; 149:91-93.
- Selroos O. Fine-needle aspiration biopsy of spleen in diagnosis of sarcoidosis. Z Erkr Atmungsorgane 1977; 149:109-111.
- Truedson H, Stjernberg N, Thunell M. Scalene lymph node biopsy. A diagnostic method in sarcoidosis. Acta Chir Scand 1985; 151:121-123.
- Brincker H. Granulomatous lesions of unknown significance in biopsies from lymph-nodes and other tissues: the GLUS-syndrome. Sarcoidosis 1990; 7:28-30.
- Hunninghake GW, Costabel U, Ando M, Baughman R, Cordier JF, du BR, Eklund A, Kitaichi M, Lynch J, Rizzato G, Rose C, Selroos O, Semenzato G, Sharma OP. ATS/ERS/WASOG statement on sarcoidosis. American Thoracic Society/European Respiratory Society/ World Association of Sarcoidosis and other Granulomatous Disorders. Sarcoidosis Vasc Diffuse Lung Dis 1999; 16:149-173.
- Fritscher-Ravens A, Sriram PV, Topalidis T, Hauber HP, Meyer A, Soehendra N, Pforte A. Diagnosing sarcoidosis using endosonography-guided fine-needle aspiration. Chest 2000; 118:928-935.
- Gal AA, Koss MN. The pathology of sarcoidosis. Curr Opin Pulm Med 2002; 8:445-451.
- Sato Y, Sasano S, Oyama K, Sakaruba M, Onuki T, Nitta S. Lung cancer associated with sarcoidosis. Jpn J Thorac Cardiovasc Surg 2003; 51:21-24.
- Wildi SM, Judson MA, Fraig M, Fickling WE, Schmulewitz N, Varadarajulu S, Roberts SS, Prasad P, Hawes RH, Wallace MB, Hoffman BJ. Is endosonography guided fine needle aspiration (EUS-FNA) for sarcoidosis as good as we think? Thorax 2004; 59:794-799.
- Agarwal R, Srinivasan A, Aggarwal AN, Gupta D. Efficacy and safety of convex probe EBUS-TBNA in sarcoidosis: a systematic review and meta-analysis. Respir Med 2012; 106: 883-892.










