Generell veileder i pediatri
3. Infeksjoner, vaksiner og undersøkelse av adoptivbarn
3.19 Vaksiner og immunglobulinprofylakse
Sist faglig oppdatert: 08.10.2025
Jacob Dag Berild, Ellen Furuseth, Kjersti Margrethe Rydland, Fredrik Skår, Berit Sofie Wiklund, Ingun Heiene Tveteraas og Margrethe Greve-Isdahl
Kapittelet omtaler sentrale temaer innenfor det norske barnevaksinasjonsprogrammet samt oversikt over anbefalte vaksiner til spesielle risikogrupper.
Følgende tema/punkter omtales:
- Barnevaksinasjonsprogrammet i Norge 2025
- Vaksinasjon av barn som får medisinsk behandling
- Vaksiner og immunglobulinprofylakse til barn i risikogrupper
- Beskrivelse av vaksiner som er anbefalt til risikogrupper
- Vaksinasjon av immunsupprimerte barn
- Allergi og vaksinasjon
- Sysvak-registrering
For utdypende informasjon om vaksiner og vaksinasjon
- Vaksinasjonshåndboka - FHI. Vaksinasjonshåndboka er delt inn i flere deler. Det inkluderer blant annet en generell del om vaksinasjon, en del om vaksinasjon ved sykdom og og en del om vaksine mot de enkelte sykdommene.
- Folkehelseinstituttets temasider om vaksiner: https://www.fhi.no/sv/vaksine/.
- Folkehelseinstituttets reiseråd: Smittevern ved reiser - FHI.
- FHIs rådgivningstelefon for helsepersonell alle hverdager kl. 13:00–14:30, tlf. 21077000 eller rådgivning pr. e-post: vaksine@fhi.no.
Barnevaksinasjonsprogrammet i Norge 2025
Tabell 1: Barnevaksinasjonsprogrammet i Norge 2025. L = levende, svekket vaksine.
| Alder | Vaksinasjon mot |
| I svangerskapet |
|
| 6 uker |
|
| 3 måneder |
|
| 5 måneder |
|
| 12 måneder |
|
| 15 måneder |
|
| 2. trinn (ca. 7 år) |
|
| 6. trinn (ca. 11 år) |
|
| 7. trinn (ca. 12 år) |
|
| 10. trinn (ca. 15 år) |
|
| Barn med foreldre fra høyendemiske land |
|
NB! Spedbarn av mødre med kronisk hepatitt B-infeksjon skal følge eget vaksinasjonsregime (posteksponeringsbehandling) frem til start av hepatitt B-vaksine i barnevaksinasjonsprogrammet, se avsnitt om hepatitt B-vaksine nedenfor.
Vaksiner til barnevaksinasjonsprogrammet utleveres gratis til helsestasjoner og andre vaksinasjonssteder (sykehusavdelinger) ved bestilling fra Folkehelseinstituttet.
Vaksinasjon av barn som får medisinsk behandling
- Det er få legemidler som interfererer med vaksiner, men det er viktig å være oppmerksom på de legemiddelgruppene hvor det er aktuelt. For intervaller mellom levende vaksiner og annen medisinsk behandling (for eksempel blodpreparater, antibiotika, hyposensibilisering ved allergi), se Vaksinasjon og samtidig bruk av andre legemidler - FHI.
- Ved vaksinasjon ved immunsupprimerende behandling, se Vaksinasjon ved immunsvikt - FHI og avsnitt nedenfor.
Vaksiner og immunglobulinprofylakse til barn i risikogrupper
Barn med ulike sykdommer/tilstander kan ha økt risiko for å bli smittet eller for alvorlige konsekvenser av sykdommen hvis de blir smittet. Disse kan dermed ha behov for flere vaksiner, se tabell under. Hver vaksine er beskrevet i mer detalj nedenfor tabellen.
Noen vaksiner til barn i risikogrupper refunderes på blå resept. Vaksiner som utleveres etter blåreseptforskriften kan ekspederes enten direkte fra Folkehelseinstituttet eller fra apotek. Resepten må påføres tydelig indikasjon, se tabell 2. For oversikt over hvilke vaksiner dette gjelder, se Bestilling og utsending av vaksiner, immunglobuliner og sera - FHI. Influensavaksine er ikke inkludert i blåreseptforskriften, men utleveres til redusert pris hver sesong til risikogrupper via kommunehelsetjenesten.
For oversikt over tilgjengelige vaksiner og immunglobuliner fra Folkehelseinstituttet, se Preparater og priser - FHI.
Nærkontakter til barn i risikogrupper og helsepersonell som jobber med syke barn, anbefales å være vaksinert mot sykdommer som barnet kan utsettes for. Aktuelle vaksiner er bl.a. sesonginfluensa, kikhoste, meslinger, og varicella, les mer om vaksinasjon av helsepersonell i Vaksinasjonshåndboka.
Tabell 2: Barn i risikogrupper og anbefalte vaksiner. L = levende, svekket vaksine.
| Risikogruppe | Vaksine mot | Refusjon på blå resept |
| Nyfødte barn av mødre med kronisk hepatitt B-infeksjon | Hepatitt B | Ja (indik.gr. A) |
Nærkontakter til personer med kronisk hepatitt B-infeksjon:
| Hepatitt B | Ja (indik.gr. A) |
| Personer under 25 år med foreldre som er født i land utenfor lavendemisk område | Hepatitt B | Ja (indik.gr. C) |
| Pasienter med tilstander som krever hyppig behandling med blod eller blodprodukter | Hepatitt A | Ja (indik.gr. D) |
| Downs syndrom | Hepatitt B | Ja (indik.gr. D) |
| Kronisk nyresvikt | Influensa | Nei |
| Kronisk leversykdom | Influensa | Nei |
| Kronisk lungesykdom og hjerte-/karsykdom | Influensa Pneumokokksykdom* | Nei |
| Diabetes mellitus | Influensa | Nei |
| Iatrogen immunsvikt | Influensa | Nei |
| Medfødt immunsvikt | Influensa | Nei |
| HIV uten symptomer | Influensa | Nei |
Manglende miltfunksjon (inkluderer splenektomerte, ved funksjonell/iatrogen påført nedsatt miltfunksjon som hereditær sfærocytose, sigdcelleanemi og kronisk ITP) | Pneumokokksykdom* | Ja (indik.gr. M) |
| Alvorlig komplementdefekt** | Meningokokksykdom | Ja (indik.gr. K) |
| Nevrologisk sykdom (nedsatt ventilasjonskapasitet) | Influensa | Nei |
| CSF-lekkasje og Cochleaimplantat | Pneumokokksykdom* | Nei |
| Gjennomgått invasiv pneumokokkinfeksjon | Pneumokokksykdom* | Nei |
| Cøliaki (komplisert sykdom) | Pneumokokksykdom* | Nei |
| Organtransplantasjon | Influensa | Nei |
| Pågående eller gjennomført kreftbehandling | Influensa | Nei |
| Gjennomført benmargstransplantasjon | Eget vaksinasjonsprogram | Ja*** (indik.gr. S)
Nei |
| Svært alvorlig fedme | Influensa | Nei |
| Annen alvorlig kronisk sykdom | Influensa | Nei |
*Det finnes flere pneumokokkvaksiner = konjugatvaksine (PKV13, PKV15, PKV20) og polysakkaridvaksine (PPV23). Se tekst nedenfor for bruk.
**Alvorlig komplementdefekt: Defekter i TCC (C5, C6, C7, C8, C9), properdin, faktor D, faktor H og C3.
***Vaksiner som inngår i barnevaksinasjonsprogrammet kan rekvireres av helsestasjon eller fastlege på vanlig måte til barn opp til 20 år.
Beskrivelse av vaksiner som er anbefalt til risikogrupper
Hepatitt A-vaksine
Vaksinen kan benyttes fra 12-måneders alder. Vaksinen kan gis som enkeltkomponent hepatitt A-vaksine, eller som kombinasjonsvaksine mot hepatitt A og B dersom pasienten også har indikasjon for vaksine mot hepatitt B.
For mer informasjon, se Hepatitt A-vaksine og normalt immunglobulin - FHI.
Hepatitt B-vaksine
Vaksine mot hepatitt B har inngått i et universelt tilbud i barnevaksinasjonsprogrammet siden 2017, mens den tidligere kun ble tilbudt barn av foreldre fra høyendemisk land. Den gis nå som en av komponentene i en kombinasjonsvaksine ved 3-, 5- og 12-månedersalder. Enkeltkomponent hepatitt B-vaksine kan gis fra fødsel. Det er egne vaksinasjonsråd ved posteksponeringsbehandling, se nedenfor.
Noen pasienter skal få undersøkt antistoffer før og/eller etter vaksinasjon mot hepatitt B. Hvilke grupper dette gjelder står i Smittevernhåndboka fra Folkehelseinstituttet: Hepatitt B-vaksine og hepatitt B-immunglobulin - FHI. For tolkning av prøvesvar se tabell 1 i Smittevernhåndboka fra Folkehelseinstituttet: Hepatitt B - FHI.
Posteksponeringsbehandling av nyfødte barn av mødre med kronisk hepatitt B
Barn av mødre med kronisk hepatitt B-infeksjon har spesielt høy risiko for selv å utvikle kronisk hepatitt B. Disse skal ha fødselsdose med enkeltkomponent hepatitt B-vaksine innen 24 timer etter fødsel, og deretter en ny dose ved 4-ukersalder før de fortsetter i det vanlige vakinasjonsprogrammet. Det er barnets utskrivende lege fra barsel som har ansvar for at beskjed om barnets risiko overbringes til helsestasjon, slik at barnet får nødvendig oppfølging etter utskrivning, inkludert 4-ukersdosen. Vaksinatør har ansvar for at vaksinering registreres i SYSVAK.
Barn som er født av mødre med kronisk hepatitt B-infeksjon, skal følge vaksinasjonsregime for posteksponeringsbehandling, og følges opp i henhold til avsnitt om perinatal Hepatitt B smitte i Nyfødtveileder. For mer informasjon, se Hepatitt B-vaksine og hepatitt B-immunglobulin - FHI.
Influensavaksiner
Barn i risikogrupper anbefales årlig vaksine mot sesonginfluensa. Vaksinering bør gis før vinterens influensasesong (dvs. perioden oktober–november). Vaksine anbefales likevel for barn i høyrisikogrupper som ikke ble vaksinert før sykdomssesongen begynte. For risikogruppedefinisjoner, se tabell ovenfor og kapittel om Influensa hos barn.
Vaksine mot influensa kan gis fra 6-månedersalder. For barn under 6-månedersalder er det ingen godkjent influensavaksine tilgjengelig, men der mødrene har blitt vaksinert i svangerskapet, kan barnet ha opptil 6 måneder beskyttelse mot influensa etter fødsel. Nærkontakter til immunsupprimerte barn anbefales årlig vaksinasjon.
Det er to aktuelle influensavaksiner til barn:
- Inaktivert (ikke-levende) injeksjonsvaksine kan gis fra alder 6 md. og oppover. Til barn under 9 år som ikke tidligere er vaksinert mot sesonginfluensa anbefales to doser med intervall på minst 4 uker. Alle andre skal ha én dose.
- Levende, svekket nasal influensavaksine kan gis til barn i aldersgruppen 2–17 år. Levende nasal vaksine er kontraindisert til barn med immunsvikttilstander, alvorlig astma eller aktivt pustebesvær, barn som bruker acetylsalisylsyrepreparater eller med ubehandlede craniofaciale misdannelser.
For barn i risikogrupper i alderen 2–17 år finnes det altså to prinsipielt ulike vaksiner å velge mellom: inaktivert (ikke-levende) injeksjonsvaksine eller nasal, levende, svekket vaksine. Forskjellen i effekt mellom vaksinene varierer fra sesong til sesong og avhenger blant annet av hvilket virus som dominerer. En vaksinetype kan derfor ikke anbefales framfor en annen. Hvilken av de to vaksinetypene som foretrekkes må vurderes av den enkelte lege og foresatte på individuelt grunnlag.
Til risikogrupper blir influensavaksine tilbudt til lav pris, og vaksinen refunderes ikke på blå resept.
For mer informasjon, se Influensavaksine - FHI.
Pneumokokkvaksiner
Det finnes flere vaksiner; 13-valent konjugatvaksine (PKV13), 15-valent konjugatvaksine (PKV15) og 20-valent konjugatvaksine (PKV20) og 23-valent polysakkaridvaksine (PPV23).
PKV har vært inkludert i barnevaksinasjonsprogrammet siden 2006, de første årene med en vaksine som beskyttet mot 7 serotyper (PKV7). Denne ble byttet ut med vaksine som beskytter mot 13 serotyper i 2011 og det er denne som fortsatt brukes. I tabell 2 er det listet opp risikotilstander for invasiv pneumokokksykdom der det kan være indikasjon for ytterligere pneumokokkvaksinering. Imidlertid er PKV13 ikke nødvendig for barn som er født etter 2011 og som har fulgt barnevaksinasjonsprogrammet i Norge, bortsett fra stamcelletransplanterte og de som har gjennomgått behandling for kreft. Det henvises til Helsedirektoratets handlingsprogram for dette (se lenker i tabell 2).
Bruk av PKV og PPV23 i kombinasjon kan være aktuelt for å gi optimal serotypedekning til pasienter med særlig høy risiko for invasiv pneumokokksykdom, f.eks. pasienter med funksjonell eller anatomisk miltmangel. De fleste barn i risikogruppene for pneumokokksykdom som er nevnt i tabell 2, vil være adekvat beskyttet gjennom konjugatvaksine i barnevaksinasjonsprogrammet, og vil ikke ha behov for både PKV og PPV23. Ved behov for både PKV13 og PPV23, bør PPV23 gis minst 8 uker etter PKV13. PPV23 er kun anbefalt til barn over 2-årsalder, da vaksinen har dårlig effekt hos yngre barn.
- Revaksinasjon/boosterdoser: Polysakkaridvaksinen PPV23 gir ikke immunologisk hukommelse, og ved fortsatt behov for beskyttelse med PPV23 anbefales revaksinasjon hvert 6. år. For personer med funksjonell eller anatomisk miltmangel kan revaksinasjon med PPV23 vurderes allerede etter 3–5 år på grunnlag av antistoffnivå i serum, men også her er hovedregelen revaksinasjon hvert 6. år. Analyse av pneumokokk-antistoffnivå i serum gjøres ved Folkehelseinstituttet, se: Mikrobiologi - FHI. Rekvisisjon: Opplysninger om problemstilling bør følge serumprøven.
Konjugatvaksine gir immunologisk hukommelse, og det er ikke nødvendig med boostervaksinasjon med PKV13.
For mer informasjon, se:
- Pneumokokkvaksine: Pneumokokkvaksine - FHI
- Vaksinasjon ved manglende miltfunksjon: Vaksinasjon og manglende miltfunksjon - FHI
Meningokokkvaksiner
Vaksine mot meningokokksykdom inngår ikke i barnevaksinasjonsprogrammet. Det finnes to ulike vaksinetyper; meningokokk ACWY konjugatvaksine som kan gis fra 6 uker/2 års alder og meningokokk B proteinvaksine som kan gis fra 2 md./10 års alder. Risikogrupper bør tilbys vaksine mot både meningokokk ACWY og meningokokk B.
- Revaksinasjon/boosterdoser: Det bør vurderes å gi boosterdose med både meningokokk ACWY og meningokokk B vaksiner etter 5 år. Ved reise til meningokokk A-endemisk område, bør boosterdose med ACWY-vaksine tilbys allerede etter 1 år.
For mer informasjon, se:
- Meningokokkvaksine: Meningokokkvaksine - FHI
- Vaksinasjon ved manglende miltfunksjon: Vaksinasjon og manglende miltfunksjon - FHI
Vannkoppevaksine
Varicella (vannkopper) kan ha alvorlig forløp hos immunsupprimerte barn. For immunfriske er risikoen for komplikasjoner ved varicellainfeksjon større med økende alder.
Vaksine mot vannkopper inngår ikke i barnevaksinasjonsprogrammet. Vaksinen kan benyttes fra 9-månedersalder. Vaksinen består av levende, svekket varicellavirus. Vaksineviruset kan gi et lett varicella-lignende sykdomsbilde hos immunfriske, mens det hos pasienter med immunsvikt er beskrevet enkelte tilfeller av alvorlig infeksjon forårsaket av vaksineviruset. Derfor er vaksinen oftest kontraindisert ved immunsuppresjon/medfødt immunsvikt.
Vaksinasjon anbefales før oppstart med immunsupprimerende behandling og før organtransplantasjon, og bør gis senest 4 uker før start av behandling eller organtransplantasjon.
Det anbefales to doser med varicellavaksine gitt med minst 6 ukers intervall for å få full beskyttelse (absolutt minimumsintervall er 4 uker). Dersom det ikke er tid til å gi begge doser før oppstart av immunsuppresjon, bør første dose likevel gis. Som hovedregel skal ikke levende, svekkede vaksiner gis etter at pasienten har startet immunsuppresjon. I noen tilfeller ved lav grad av immunsvekkelse kan det likevel vurderes å tilby enkelte levende svekkede vaksiner til utvalgte pasienter (1-4). Eventuell vaksinasjon under pågående immundempende behandling må må vurderes og besluttes av behandlende spesialist ut fra gjeldende anbefalinger i fagmiljøene.
For mer informasjon, se Vaksine mot vannkopper (varicella) - FHI.
Anbefalinger for profylakse etter eksponering for vannkopper
Det finnes to alternativer som kan benyttes som postekspoeringprofylakse; antiviral behandling (aciklovir/valaciklovir) eller VZIG (immunglobulin mot VZV). For mer informasjon, se avsnitt om Varicella/Herpes zoster hos barn ved immunsuppresjon, transplantasjon og kreftbehandling.
For personer med immunsvikttilstander utleveres vannkoppevaksine og VZIG etter bestemmelsene i Blåreseptforskriften §4. Det er ingen refusjonsordning for vannkoppevaksine eller VZIG til andre grupper.
Vaksine og VZIG på blå resept rekvireres fra apotek eller Folkehelseinstituttet. VZIG utleveres bare på spesielt godkjenningsfritak. Immunglobulin må gis så raskt som mulig etter smitteeksponering, og bør rekvireres per telefon fra Folkehelseinstituttet, se kapittel om bestilling av vaksiner, immunglobulin og sera/antitoksin i vaksinasjonshåndboka for helsepersonell - FHI.
Oversikt over tilgjengelige preparater og priser blir kontinuerlig oppdatert på nettsiden Preparater og priser - FHI.
For mer informasjon, se: Varicellavaksine (vannkopper) og varicella-zoster immunglobulin – håndbok for helsepersonell - FHI.
Vaksinasjon av immunsupprimerte barn
Hovedprinsipper for vaksinasjon ved nedsatt immunforsvar:
- Formålet med vaksinasjon er å gi best mulig beskyttelse med minst mulig bivirkningsrisiko.
- Grad av immunsuppresjon påvirker en persons sårbarhet for infeksjoner og behov for beskyttelse gjennom vaksinasjon.
- Behandlende lege har ansvar for vurderingen vedrørende vaksinasjon av personer med nedsatt immunforsvar.
- Levende vaksiner:
- Levende, svekkede vaksiner kan gi alvorlig infeksjon hos personer med nedsatt immunforsvar og er derfor som hovedregel kontraindisert.
- Vaksinasjon bør vurderes før oppstart av immundempende behandling.
- Dersom det er sterk indikasjon for vaksine hos pasienter som bruker immundempende behandling, kan vaksinasjon gjøres etter pause i behandlingen, se figur 1.
- Ikke levende-vaksiner:
- Personer med nedsatt immunforsvar kan vaksineres med ikke-levende vaksiner, men kan ha redusert effekt av vaksinene. De kan også ha dårligere beskyttelse av tidligere gitte vaksiner.
- Personer med nedsatt immunforsvar har ofte lavere antistoffrespons på vaksiner, men får likevel oftest boostereffekt eller serokonversjon (tydelig antistoffrespons) ved vaksinasjon. Dette kan avhenge av grad av immunsuppresjon.
- Det kan derfor være behov for ekstra doser, og/eller høyere dosering og kortere intervall mellom ev. revaksinasjoner.
- Tross korrekt vaksinering, oppnås likevel ikke full beskyttelse hos alle, og pasientene bør informeres om dette. Mistanke om risiko for dårlig vaksinerespons utgjør ikke kontraindikasjon mot en ikke-levende vaksine som er indisert.
Figur 1
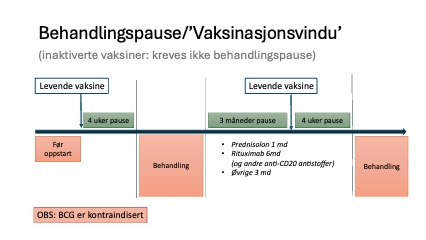
Kontakt Folkehelseinstituttets vaksinerådgivning ved behov for nærmere råd.
Se vaksinasjonshåndboka til FHI for utfyllende informasjon: Vaksinasjon ved immunsvikt - FHI.
Allergi og vaksinasjon
Alvorlige allergiske reaksjoner på vaksine er sjelden. De fleste personer med allergi reagerer ikke på stoffer som finnes i noen av vaksinene. Hovedregelen er derfor at personer med allergi kan og bør vaksineres på samme måte som alle andre.
Vanligvis vil alvorlig straksallergisk reaksjon på en vaksine eller innholdsstoffer i en vaksine utgjøre kontraindikasjon mot å gi flere doser av samme vaksine. Hvis en person som tidligere har opplevd alvorlige straksallergiske vaksinereaksjoner har behov for ny dose med samme type vaksine, må nytten ved vaksinasjon i det konkrete tilfellet vurderes mot risikoen for en alvorlig allergisk reaksjon.
Personer som tidligere har reagert anafylaktisk i andre sammenhenger (uansett agens), kan ha økt risiko for straksallergisk reaksjon på nye stoffer. I slike tilfeller bør derfor vaksinasjon utføres under utvidet allergiberedskap med lege tilgjengelig og forlenget observasjonstid.
Les mer i Vaksinasjonshåndboka: Vaksinasjon av personer med allergi - FHI.
Sysvak-registrering
Det er meldeplikt for alle vaksiner gitt i Norge, jf. SYSVAK forskriften §2–1. Vaksinatør skal i henhold til forskrift opplyse om registrering av vaksinasjonsstatus i SYSVAK-registeret ved vaksinasjon.
For mer informasjon, se: Informasjon til helsepersonell - FHI.
Samhandling
Behandlende lege har ansvar for å informere fastlege og helsestasjon ved tilpasninger av vaksinasjonsprogrammet eller behov for vaksiner utenom vaksinasjonsprogrammet. Det må informeres om navn på preparat, antall doser og intervaller som er nødvendig. Dessuten må det informeres om eventuelle kontraindikasjoner for vaksiner.
For barn av mødre med kronisk hepatitt B-infeksjon, er det utskrivende leges ansvar å gi tydelig informasjon til rett tid (dvs. i god tid før 1-månedsalder) til fastlege og helsestasjon om videre oppfølging av barnet, se avsnitt ovenfor.
Referanser
- Posfay-Barbe KM, et al. Varicella-zoster immunization in pediatric liver transplant recipients: safe and immunogenic. Am J Transplant 2012; 12:2974-85.
- Suresh S, et al. Live vaccines after pediatric solid organ transplant: proceedings of a consensus meeting, 2018. Pediatr Transplant 2019; 23:e13571.
- Danziger-Isakov L, et al. Vaccination of solid organ transplant candidates and recipients: guidelines from the American Society of Transplantation Infectious Diseases Community of Practice. Clin Transplant 2019; 33:e13563.
- Piché-Renaud P-P, et al. Safety and immunogenicity of the live-attenuated varicella vaccine in pediatric solid organ transplant recipients: a systematic review and meta-analysis. Am J Transplant 2023.
Tidligere versjoner
Versjon 2006: Claus Klingenberg og Hanne Nøkleby
Revidert 2009: Hanne Nøkleby og Claus Klingenberg
Revidert 2015: Hanne Nøkleby og Claus Klingenberg
Revidert 2018: Ellen Furuseth, Margrethe Greve-Isdahl og Sara Viksmoen Watl










