Nyfødtveileder
5 Lunge og respirasjon
5.18 Høyfrekvensventilering
Sist faglig oppdatert: 05.03.2022
Per Ivar Kaaresen, Claus Klingenberg, Arild Leknessund, Jannicke H. Andresen og Hans Jørgen Guthe
Bakgrunn
- Høyfrekvensventilasjon (HFV) er mekanisk ventilasjon som bruker et konstant distensjonstrykk (mean airway presure [MAP]), med trykkvariasjoner som svinger (oscillerer) rundt MAP med høy hastighet (frekvens). På denne måten blåses alveolene opp med et mere konstant trykk uten stor forskjell i inspirasjons- og ekspirasjonsfase.
- Ved HFV genereres små tidalvolumer, som ofte er mindre, lik eller kun litt større enn fysiologisk dødvolum (2,0–2,5 ml/kg).
- Tidalvolumer ved HFV (VThf) leveres vanligvis med frekvenser mellom 5–15 Hz (1 Hz = 60/min), dvs frekvenser på 300–900/min.
- En pasient som er spontant pustende kan fint puste på toppen av HFV.
- Oppsummering av lungefysiologi og gassutveksling ved HFV finnes i referanse 1 og 9.
Oksygeneringen ved HFV bestemmes av lungevolumet, og er primært bestemt av MAP.
- Justering av MAP er den viktigste måten å bedre/endre oksygenering
- MAP ved HFV settes ofte 2–4 cm over det MAP man hadde på konvensjonell respirator pga behov for å rekruttere mest mulig lungevev. Noe forsiktighet ved økning av MAP ved MAS. Ved luftlekkasje og lungehypoplasi settes MAP initialt likt eller lavere enn MAP ved konvensjonell respirator, og man aksepterer noe høyere FiO2.
Ventilasjonen (CO2 utluftingen) ved HFV bestemmes av DCO2 = frekvens x VThf2.
Følgende innstillinger påvirker DCO2:
- Amplitude (delta P): Et mål på kraft på oscillasjonene, som igjen styrer tidalvolumene (VThf)
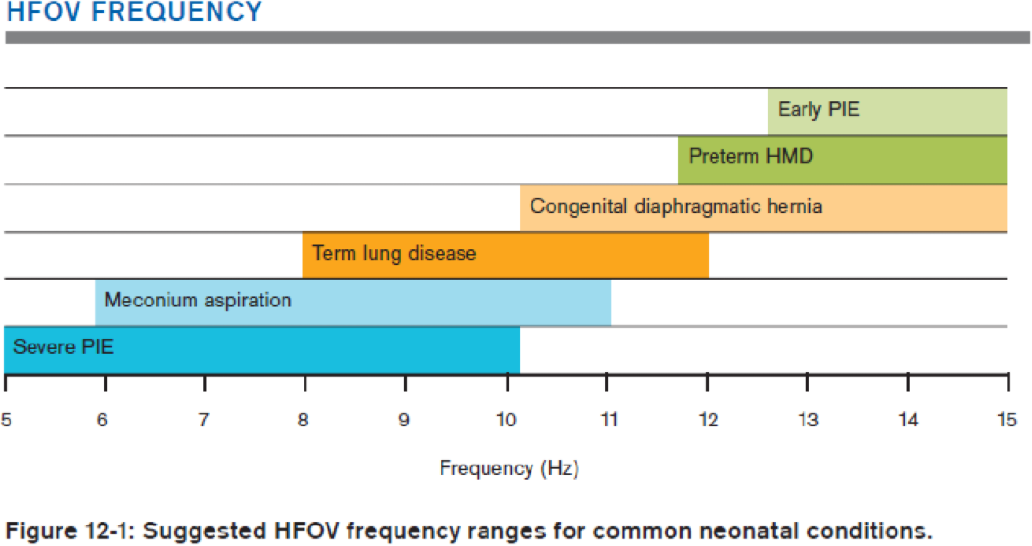
- Frekvens (Hz): Økning av frekvens (ved vanlig HFV) gir relativt sett reduksjon i VThf og medfører derfor en reduksjon av utlufting. Motsatt vil reduksjon i frekvens gi økt utlufting (NB. forholdet mellom frekvens og CO2 utlufting er motsatt av konvensjonell ventilasjon). Økt amplitude er normalt mere effektivt enn reduksjon i frekvens for CO2 eliminasjon. Det er trolig mere skånsomt for lungene med høye frekvenser. For premature ønskes frekvenser fra 10–15 Hz for mest mulig skånsom ventilasjon/minimere amplitude-påvirkning på terminalt luftveier. Ved svært stive lunger kan frekvens reduseres gradvis ned mot 5 Hz under nøye overvåking av CO2. Se ellers figur under for vurdering rundt type lungesykdom og valg av frekvens (Pillow J, Drager HFOV-manual 2016).
Ratio inspirasjonstid/ekspirasjonstid (I:E-ratio)
- Det anbefales oftest å starte med ratio 1:2 (svarende til 33 % inspirasjonstid), altså med en litt lengre ekspirasjonstid som teoretisk kan forebygge air trapping.
- Man oppnår imidlertid mere kraft ved å gå fra 1:2 til 1:1 ratio, slik at hvis man har problemer med å oppnå ønsket amplitude kan det være «nødvendig» på noen respiratorer, se under, å gå over til 1:1 ratio.
- Ved HFV uten VG: En ratio på 1:1 gir et større tidalvolum enn 1:2(–3) ratio, noe som gir økt utlufting (jfr at man får bedre amplitude).
- Ved HFV med VG: Her vil antagelig en endring av I:E ratio ha en annen effekt da tidalvolumet er fast. En I:E ratio på 1:2 kan da gi bedre utlufting enn 1:1. Dette vil nok og være avhengig av grad av lungesykdom og valg av respirator
NB1: Effekt av oscillasjon vil også være avhengig av størrelse på pasient (jo lenger luftvei, jo høyere amplitude nødvendig), størrelse på tube (amplitudetap gjennom liten tube) og compliance i utstyr/slangesett (myke slanger reduserer effekt av oscillasjonene).
NB2: Dräger Babylog VN500 genererer ikke nok kraft ved høye frekvenser til å gi høye amplituder. Det kan derfor måtte gjøres justeringer på frekvens når man øker amplitude, slik at amplituden oppnås. Om dette er nødvendig vil man kunne se hvis man følger gitt amplitude på displayet etter justering. Man kan også oppnå større kraft ved å endre ratio til 1:1.
NB3: Det omvendte forholdet mellom frekvens og ventilasjon som man ser ved «klassisk» HFV, gjelder ikke lenger hvis man bruker HFV+ VG. Da vil tidalvolumet holdes konstant ved at amplituden fortløpende justeres. Og ved konstant tidalvolum vil en økning/reduksjon i frekvens gi samme effekt på ventilasjon som ved konvensjonell respiratorbehandling.
Volumgaranti (VG)
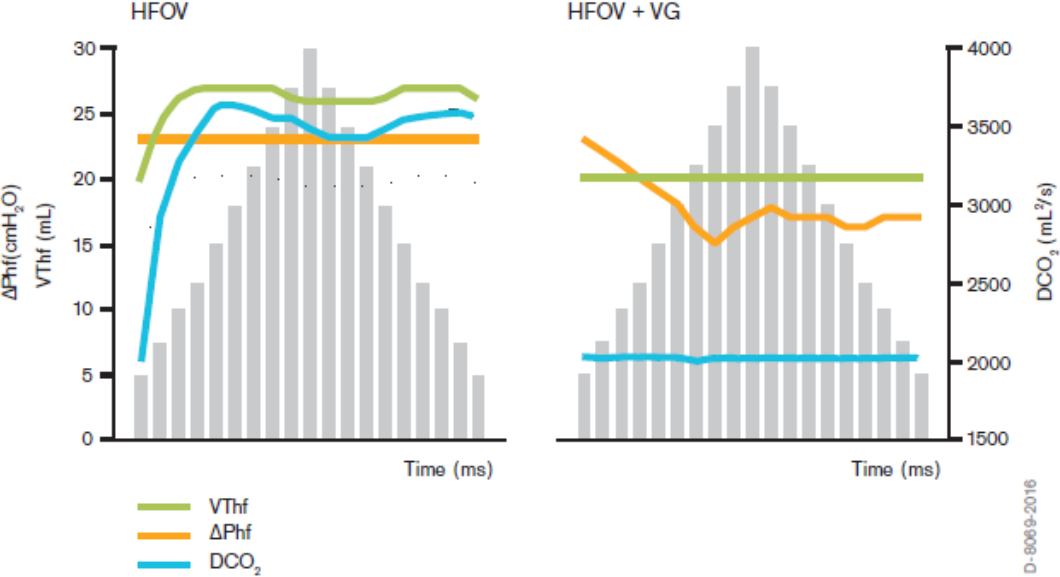
Ved bruk av VG ved HFV får man altså et stabilt tidalvolum, med konstant DCO2 og varierende amplitude. Dette gjør at man får mindre variasjon i utlufting ved slimmobilisering, inhomogene lunger og pasient/respirator-interaksjoner som gjør at compliance kan endre seg under pågående oscillering. Se bildet under for illustrasjon (Dräger HFOV manual 2016)
- Godt samsvar mellom VThf og pCO2.
- Færre hypo- og hyperkapni episoder i kliniske studier
- Manglende data på langtidsutkomme
- Holdepunkter for at de fleste premature vil trenge < 2 ml/kg i VG, sjelden > 2,5 ml/kg. Men tidalvolumet er best satt etter en tilfredsstillende blodgass hvor volum er notert ved blodprøvetaking.
- Justeringer av volum gjøres i små intervaller (0,1 ml/kg)
- Amplitude stilles ca 10 over den «brukte» amplituden
- Økt frekvens ved HFV+VG gir økt utlufting:
→ Ved HFOV med volumgaranti er Vthf konstant
→ DCO2 = Frekvens x Vthf x Vthf - Lekkasjen kan ikke være for stor ved VG, det finnes ingen studier eller data på eksakt cut-off, men erfaringsmessig blir det vanskelig å bruke VG ved lekkasje > 50 %.
DCO2 = frekvens x VThf2
- DCO2 er markør på alveolær ventilasjon som kan avleses på respiratoren. Gir en indikasjon på grad av ventilasjon og kanskje bedre enn visuell bedømmelse av hvor mye barnet «rister». Typisk mål på DCO2 vil være 40–80 ml/kg, men man må huske at den «riktige» DCO2verdien vil være individuell for hver pasient og kan variere fra under 40 ml/kg til verdier langt over 80 ml/kg.
- Fall i DCO2 indikerer redusert compliance/økt motstand (sykere lunger, slimplugger) eller luftlekkasje (VThf faller). Man må også tenke på aksidentell ekstubasjon.
- Økende DCO2 kan indikere bedring i compliance.
- Estimat av CO2 utlufting skjer ved trykksensor, altså utenfor pasient (ved konvensjonell respirator +VG er VG mer lik det som skjer på alveolenivå).
- DCO2 verdi er kun relevant å monitorere hvis man bruker HFV uten VG. Ved bruk av HFV med VG vil DCO2 være på konstant nivå (definisjonsmessig), men man kan da se på endringer i amplitude over tid med tanke på om det er bedring eller forverring.
- Ved stor lekkasje kan DCO2 være upålitelig med store variasjoner som ikke nødvendigvis gjenspeiler ventilasjon
Respiratorer for HFV
Det foreligger ingen klinisk sammenliknende studier mellom ulike HFV-respiratorer, men det er kun studier der Sensormedics, som er en ren HFV-respirator, er benyttet og som har vist positive effekter sammenliknet med konvensjonell behandling.
Hos premature barn med RDS er konvensjonelle respiratorer med HFV funksjon med all sannsynlighet allikevel bra nok.
For fullbårne/større barn og tilstander med stor risiko for air-trapping kan det ev. oppstå tilstander der konvensjonelle respiratorer med HFV funksjon ikke er tilstrekkelige kraftige. Flere universitetssykehus har Sensormedics HFV for slike tilfeller. Ved oksygeneringssvikt og/eller ventileringssvikt til tross for maksimal innsats (inkl. iNO) vil det trolig være indikasjon for ECMO.
Oppsett HFV på konvensjonell respirator
Noen maskiner krever et annet slangesett for oscillering, men andre kan bruke det samme ved HFV som ved konvensjonell. De fleste gir et mål på DCO2 som kan avleses på skjermen. Etter hvert tilbyr også de fleste respiratorer volumgaranti-funksjonen (VG). Man må alltid være oppmerksom og se at maskinen gir den innstilte amplituden.
Oppsett Sensormedics HFV
Sensormedics er en kraftig oscillator, med en piston som genererer oscillasjonene. Den er avhengig av stive, relativt korte slanger, og barna (og sengene) må posisjoneres i henhold til dette. Det er viktig å være oppmerksom på at CO2 kan falle fort ved overgang fra HFV på konvensjonell respirator til Sensormedics. I utgangspunktet stilles inspirasjonstiden på 33 %, flow på 15 (–20), og MAP, frekvens og amplitude som på konvensjonell respirator. Flow kan økes ved oksygeneringsproblemer, og ved høye amplituder (>70). Endring av flow vil endre MAP og denne må justeres til ønsket nivå.
Er HFV nyttig?
De fleste studier vedrørende elektiv HFV behandling er gjort på premature med homogen lungesykdom (RDS). På tross av lovende dyreeksperimentelle studier har de kliniske studiene vært motstridende. Cochrane analysen fra 2015 antyder:
- Muligens litt lavere forekomst av BPD ved bruk av HFV versus konvensjonell respirator, men usikre funn pga sprikende resultater/heterogenitet.
- Noe økt forekomst av luftlekkasje ved bruk av HFV.
- Det er ingen andre større fordeler/ulemper identifisert på kort eller lengre sikt.
HFV synes trygt og nyttig i trenede hender, men det er ikke grunnlag for å anbefale elektiv bruk av HFV hos premature (fremfor vanlig konvensjonell respirator).
HFV kombinert med VG kan kanskje være fordelaktig på små skjøre lunger når man kombinerer lavere VG og høyere frekvens.
Bruken av HFV som «rescue» behandling ved ulike tilstander er også dårlig dokumentert, uten noen større randomiserte studier hos premature og fullbårne. Det foreligger derimot en rekke observasjons-studier, noen mindre randomiserte studier, samt klinisk erfaring som tyder på at HFV kan være livreddende i vanskelige situasjoner.
Indikasjon for HFV ved fleste Nyfødtavdelinger er gjerne «tidlig rescue» hos pasienter der konvensjonell respiratorbehandling er vanskelig eller ikke gir tilfredsstillende resultat. Det finnes imidlertid også noen store nyfødtavdelinger i utlandet som velger HFV som primærbehandling ved RDS fremfor konvensjonell respiratorbehandling, og med gode resultater.
Indikasjoner for bruk av HFV
Primærbehandling av premature
De fleste nyfødtavdelinger i Norge har tradisjon for å starte med konvensjonell respiratorbehandling, og bruker ikke HFV som primærbehandling ved RDS. Det er imidlertid noen store sentra (f.eks Amsterdam og Stockholm) som bruker HFV som primærbehandling med gode resultater.
Rescue-behandling ved alvorlig RDS hos premature
Indikasjoner kan være: FiO2 > 0,40–0,50 på tross av surfactant og «optimalisert» konvensjonell behandling med PEEP 7–8 cm H2O. Nedsatt luftholdighet ved rtg thorax samt behov for høye trykk (PIP > 25 cm H2O) for å oppnå ønskede tidalvolumer, forsterker indikasjonen. Ved mistanke om lungehypoplasi (PPROM) bør man starte tidlig. I tillegg må man da også være forberedt på pulmonal hypertensjon og ha NO-gass klart/oppkoblet.
Mekoniumaspirasjons syndrom (MAS)
Komplisert tilstand karakterisert med atelektaser + obstruksjon (VQ mismatch/intrapulmonal shunting). Indikasjon for høye MAP trykk. Imidlertid ofte også PPHN (sekundært til acidose) med hø-ve shunting over duktus 🡪 ikke sikkert man får vesentlig effekt av høy MAP. Det er risiko for overdistensjon og påfølgende sirkulatorisk påvirkning. HFV i startfasen er derfor noe omstridt og noen venter (om mulig) til etter 48 timer da lungesykdommen har et mer homogent preg pga. pneumonitten. Mange avdelinger i Norge har gode erfaringer med å starte tidlig ved FiO2 > 0,50–0,60 på tross av surfactant og utbredte lungeforandringer. Ofte foreligger PPHN og kombinasjonen HFV og NO gass er ofte gunstig/nødvendig.
Persisterende luftlekkasje (pneumothorax, PIE)
Når det er behov for middeltrykk (MAP) > 10–12 cm H2O, særlig ved PIE.
Respirasjonssvikt av andre årsaker
Ved oksygenerings- eller ventilasjonsproblemer uansett årsak, antydningsvis PaO2 < 6,7 kPa og/eller PaCO2 > 8,5 kPa med FiO2 >0,80 på tross av optimal konvensjonell behandling og/eller OI* >20–25. Ved PPHN med lite uttalt parenkym-forandringer på rtg toraks og tegn til ekstrapulmonal shunting (ductus/foramen ovale) starter en ofte først med NO (obs. utelukk hjertefeil). Forsiktighet ved obstruktiv lungesykdom (etablert BPD, RS-virus infeksjon) pga risiko for air-trapping, dog er det også rapportert god effekt ved RS-virus-infeksjoner.
Relative kontraindikasjoner mot HFV
Pasienter som er hypotensive enten som følge av hypovolemi eller dårlig myokardfunksjon tolererer oftest HFV dårlig og kan bli svært ustabile. Vurder kardiovaskulær status: ekkokardiografi, perifer sirkulasjon (kapillær refill), laktat, urinproduksjon og blodtrykk før oppstart. Korriger hypovolemi og/eller start pressor om nødvendig. Spesielt viktig hos pasienter med sepsis, MAS, PPHN.
Før oppstart HFV
- Transkutane pO2/pCO2 og SpO2 skal alltid etableres først.
- NAK/perifer arteriekran for kontinuerlig BT og blodgasser er sterkt ønskelig. Dersom dette ikke er mulig følges BT med non-invasiv måling, hyppig i starten (5–10 min), senere sjeldnere utfra klinikken.
- Et sentralt venekateter (NVK over/i diafragmanivå) er ønskelig for å kunne gi pressor og evt. måle CVP.
- Vurder tubestørrelsen, større tube= større effekt. Ved stor lekkasje fra tuben under konvensjonell behandling, bør tuben som regel skiftes.
- Lukket sugesystem. Sug godt i tuben/trakea før oppstart.
Prinsipper for HFV – strategier og settinger avhenger av diagnosen!
PRIMÆRBEHANDLING AV RDS HOS PREMATURE
- Strategi vil være skånsom ventilasjon.
- Start med MAP ofte rundt 8 cm H2O
- Frekvens 12–15 Hz
- I:E ratio 1:2
- Amplitude som gir pCO2 rundt 6 kPa. Tilstreb at barnets thorax rister, man følger PCO2 og avleste tidalvolum (se under HFV+VG for mål for tidalvolum), og kan f.eks starte med en amplitude rundt 15 som økes ved behov.
- Ved bruk av HFV+VG foreslås start på 1,5–1,8 ml/kg.
- Ved mangelfull oksygenering økes MAP trinnvis (1 cm H2O av gangen) til barnet oksygenerer adekvat.
«RESCUE BEHANDLING» VED ALVORLIG RDS
Hovedstrategien er å åpne atelektatiske terminale luftveier/alveoler og holde dem åpne ved hjelp av høy MAP; såkalt volumrekrutterende strategi. Kun en slik strategi er dokumentert effektiv ved RDS.
- Frekvensen settes til 10 Hz (opp mot 15 Hz hos de minste).
- Amplitude man tilstreber at barnets thorax rister, man følger tcPCO2 tett og avleste tidalvolum (se under), og kan f.eks starte med en amplitude rundt GA i uker.
- FiO2 som ved konvensjonell behandling
- MAP (PEEP) settes 3–4 cm H2O over MAP-trykket som ble brukt ved konvensjonell behandling.
- Gjør rekrutteringsmanøver (se under) hvis oksygeneringen ikke er adekvat. Dersom en ikke får noen effekt på SpO2 ved å øke MAP-trykket 6 cm H2O, bør en skifte tilbake til konvensjonell respirator igjen. Revurder diagnosen, lungestatus (rtg thorax), vurder den kardiovaskulære situasjon (volum/pressor?), vurder NO-gass evt. i kombinasjon med HFV og forsøk evt. igjen.
- Sjekk rtg thoraks etter 1–2 timer for å bedømme lungevolumet. Ved et optimalt lungevolum skal diafragma stå ved Th8-9, lungene vise bedret luftholdighet, men uten tegn til hyperinflasjon.
Amplituden økes til barnet rister tydelig og/eller pCO2 begynner å falle. Se på DCO2, jmf innledning og at VThf ligger rundt 1,6–2,2 ml/kg. Obs. ved bedret compliance/lungevolum får man mer effekt av oscillasjonene og amplituden må reduseres – viktig for å unngå hyperventilasjon! I en studie fant man at en endring i amplituden på 3 cm H2O førte til en median endring i pCO2 på 1 kPa (men med store variasjoner) og at 95 % av endringene skjedde ila 30 minutter.
Det anbefales å vurdere og bytte over til HFV + VG etter 30–60 min da dette gir mere stabile pCO2-verdier og kan gjøre det enklere å styre behandlingen.
PERSISTERENDE LUFTLEKKASJE
Her er hovedstrategien å bruke lavest mulig trykk for å holde akseptable blodgasser. En forsiktig/lett lungekollaps aksepteres. Diafragmanivå rundt Th8
- Forsiktig bruk av MAP, start lik/under nivå ved konvensjonell respirator
- Høy frekvens 10–15 (premature) Hz
- I:E ratio 1:2–3 (Endring fra 1:2–1:3 vil redusere tid med høyest trykk og kan redusere lekkasje)
- MAP så lav som mulig så lenge FiO2 0,7–0,8. Forsøk å redusere til luftlekkasje stopper, konservere 1–2 døgn så rekruttere opp igjen forsiktig til akseptabel FiO2 < 0,4 (Se avsnitt Avvenning fra HFV).
- Aksepter SpO2 ned mot 88 %/PaO2 ned mot 6 kPa
- Amplitude: justeres slik at barnet rister, men aksepter noe mindre risting og tilstreb pCO2 opp mot 8–9 kPa så lenge pH >7,25.
MEKONIUMASPIRASJONSYNDROM
Ved MAS er det ofte gunstig å bruke noe lavere frekvenser enn ved homogene lungesykdommer.
Ved tendens til air-trapping, inhomogent bilde:
- Frekvens 5–8 Hz
- MAP lik MAP ved konvensjonell
- Amplitude ved start HFV er avhengig av lungesykdom. Man kan pragmatisk starte med amplitude rundt GA i uker (35–40), men juster amplitude slik at barnet rister godt og følg tett CO2 og tidalvolum
Ved mer diffust ARDS-liknende bilde:
- Frekvens 6–10 Hz
- MAP 2–4 cm H2O over konvensjonell
- Amplitude; som over.
LUNGEHYPOPLASI (POTTER, LANGVARIG PREMATUR VANNAVGANG)
Disse pasientene har lite lungevev ut fra kroppsstørrelse, og derfor lite rekrutterbart lungevev. Stor fare for lungeskade, skånsom ventilasjon:
- Frekvens 10–15 Hz
- MAP lik konvensjonell MAP, økes til maks 14–15 cm H2O, høyere dersom samtidig RDS. Øk i 1 cm H2O-intervaller inntil SpO2 begynner å stige. Behold dette trykket, reduser FiO2 gradvis, deretter vanlig avvenning
- Amplitude ved start HFV. Start gjerne rundt GA i uker, men tilstreb minste grad av risting med mål om normal pCO2. Unngå acidose som forverrer ev. PPHN, vurder tillegg av NO-gass som ofte har god effekt (se egen prosedyre)
MEDFØDT DIAFRAGMAHERNIE
Se kapittel Medfødt diafragmahernie.
I utgangspunktet skal disse barna transporteres til Trondheim eller Oslo (se egen prosedyre).
Det er ikke vist at HFV er bedre enn konvensjonell respirator! I situasjoner der barnet vurderes ikke-transportabelt kan det være aktuelt med HFV/NO. På samme måte som ved lungehypolasi har disse barna lite rekrutterbart lungevev. Stor fare for lungeskade, skånsom ventilasjon:
- Frekvens 10 Hz
- MAP lik eller 1–2 cm H2O over konvensjonell (avhenger av den kontralaterale lunge som skal ha normal inflasjonsgrad). Unngå aggressiv rekruttering, jfr. lungehypoplasi over. Bruk MAP trykk 14–16 cm H2O, ikke over 20 H2O.
- Amplitude ved start HFV. Man kan pragmatisk starte med amplitude rundt GA i uker (35–40), justeres videre slik at barnet rister og barnet har pCO2 i målområdet 6,5–8,5 kPa, i henhold til prosedyre om medfødt diafragmahernie.
Rekruttering
Ved økende oksygenbehov/fallende SpO2 kan det være indikasjon for å rekruttere.
Det er publisert studier som viser at rekruttering er trygt og ikke gir mer luftlekkasje, men det foreligger ikke mye dokumentasjon. Noen senter bruker mye rekruttering, mens andre er tilbakeholdne.
Ved rekruttering økes MAP i 1–2 cm H2O intervaller inntil SpO2 stiger/oksygen kan reduseres. Man bør bruke 5 – 15 minutter per økning. En studie har vist at det tar ca 5 minutter for en prematur lunge å stabilisere seg etter økt MAP, og ca 10 minutter for et terminfødt barn. Ved sterkt nedsatt compliance vil det antagelig ta > 10 minutter også for premature.
Dersom forbedringen i oksygenering stopper opp, skal en ikke øke ytterligere, men sjekke lungevolumet (rtg thoraks). Dersom pasienten blir ustabil med økende oksygenbehov, stigende CO2, eller BT-problemer, kan dette være tegn på hyperinflasjon og MAP reduseres med 1–2 cm H2O. Når FiO2 faller ned til 0,3–0,4 (ved MAP i nivåene 10–15 cm H2O) har en oftest oppnådd normalt lungevolum. En kan da ofte redusere MAP med 1–2 cm H2O uten å miste noe lungevolum. Ved høye MAP (>18–20 cm H2O) begynner en å redusere MAP forsiktig når FiO2 <0,6, ellers er risikoen for hyperinflasjon stor.
Gjentatt suging (også med lukket system) kan føre til små atelektaser og sekretstagnering hvor kortvarig re rekrutering av lungene kan oppnås ved å legge inn sukke-funksjon med 1–5 sukk per minutt. Avdelinger har også positiv erfaring med at sekretstagnasjon ved lengre tids HFO behandling kan bedres ved å legge inn fem sukk per minutt, med Ti 0.5 sek og PIPsukk på 7 cmH2O over MAP.
Hvis SpO2 stiger: Reduser først FiO2 gradvis ned mot 0,6–0,3 avhengig av MAP-trykket man bruker. Deretter nedtrapping av MAP.
Monitorering ved HFV
Rtg thoraks.
I praksis beste måte å kontrollere lungevolumet og spesielt om det er tendens til hyperinflasjon. Diafragma skal som hovedregel stå ved Th 8–9 (høyre mcl). Hyperklare lunger, avflatet diafragmakuppel, lite hjerte sammen med diafragmagrenser lavere enn Th 9, tyder på hyperinflaterte lunger og MAP-trykket må senkes. Ved lungehypoplasi gjelder ikke disse grensene og man må utvise skjønn og se på oksygenbehovet.
Vær spesielt oppmerksom på sammenhengen mellom lungevolum og PaO2: Oksygeneringen bedres ved økende lungevolum opptil normalt volum. Ved økende volum utover dette blir lungene hyperinflaterte og PaO2 vil falle (og pCO2 kan stige). I en slik situasjon skal MAP-trykket senkes og ikke økes. Det siste vil øke hyperinflasjonen og ytterligere forverre PaO2.
Ved «tette» lunger, utbredte infiltrater (atelektaser) og oksygeneringsproblemer, må man øke MAP-trykket ytterligere, selv om lungegrensene er ved Th9. Når optimalt lungevolum er oppnådd, kan en ofte redusere MAP 1–2 cm H2O uten å tape noe lungevolum. Oksygenbehovet gir også en pekepinn: FiO2 < 0,3 indikerer et tilfredsstillende lungevolum. Dersom lungene virker hyperinflaterte på tross av at MAP-trykket er redusert kan det foreligge air-trapping. Frekvensen senkes. Samtidig må som regel amplituden også reduseres for å unngå hyperventilasjon (større tidalvolum).
Hyppig rtg thoraks er indisert i starten – spesielt viktig ved oksygenerings-problemer og når en er usikker på om dette skyldes atelektatiske eller hyperinflaterte lunger. Ta da f.eks rtg 1–2 og 6 timer etter oppstart, deretter hver 12–24 time. Dette må avpasses klinikken. Ved raske/store endringer av amplitude/MAP, må en være liberal med rtg thoraks.
Blodtrykk
Vær spesielt oppmerksom på blodtrykksfall (særlig hos pasient som i utgangspunktet var hypovolemisk) som følge av økt intratorakalt trykk og dermed kompromittert venøs retur og nedsatt cardiac output (CO). Asfyktiske pasienter (myokarddepresjon) får også oftere BT-problemer. Hyperinflaterte lunger kan gi BT-fall. Kardial dekompensasjon er særlig beskrevet hos septiske pasienter. Redusert CO kan gi oksygeneringsproblemer og tiltaket er å gi volum/pressor framfor øking av MAP. Økt hjertefrekvens, forlenget kapillær refill tid, redusert urinmengde og evt. økende CVP styrker behandlingsindikasjonen. Vedr. volum/pressor, se kapittel om Hypotensjon og hypoperfusjon.
Avvenning fra HFV
Homogene lungesykdommer (RDS)
Når et optimalt lungevolum er oppnådd (rtg thoraks Th 8–9) og FiO2 er redusert til 0,3–0,4 kan nedtrapping begynne. Ved svært høye trykk rundt 18–20 eller høyere reduserer man vekselvis på trykket og FiO2 når man kommer ned i FiO2 på ca 0,6. Vær imidlertid oppmerksom på at ettersom mere av lungen åpnes og compliance bedres, kan en få et økende lungevolum med samme trykk (“silent recruitment”). Hvis en ikke oppdager dette vil lungene bli hyperinflatert og oksygeneringen forverres.
Nedtrappingen foregår ved å redusere MAP 1 cm H2O ad gangen med 2–4 timers intervaller. Av og til raskere, spesielt ved rask bedring av lungesykdommen må man holde tritt for å unngå hyperinflasjon. Går man for raskt fram vil lungen kollabere, oksygen-behovet stiger og MAP-trykket må økes, ofte til samme nivå eller litt over det en hadde da nedtrappingen begynte.
Dersom man er i tvil om oppståtte problemer skyldes hyperinflasjon/kollabering må man sjekke med rtg thorax. Man kan ev. forsøke å redusere MAP med 3–4 cm H2O: Dersom SpO2 stiger tyder dette på at hyperinflasjon var årsaken til problemet, fallende SpO2 tyder på at MAP-trykket skal økes.
Når MAP-trykket er ≤ 10 cm H2O og FiO2 under 0,3 kan man vurdere ekstubasjon til CPAP. Dette vil avhenge av egenrespirasjonen. Enkelte ganger bør man avvenne via konvensjonell respirator. Vær oppmerksom på at når en kommer ned i lave trykk kan slimproblemer oppstå og det kan da lønne seg å gå over til AC med VG framfor stadig suging. Evt. legge på «sukke-funksjon», se under rekruttering.
Luftlekkasje/inhomogene lungesykdommer
Her prioriteres trykkreduksjoner på bekostning av FiO2. Når FiO2 er redusert til 0,7–0.8, starter man reduksjon av MAP. Oppretthold normal/lavt lungevolum (Th 7–8). Når luftlekkasjen har vært borte i 48 timer kan man bruke framgangsmåte som ved RDS.
MAS får også et mer homogent preg etter 48 timer og man bruker samme strategi som ved RDS.
Spesielle problemer ved HFV
- Volumgaranti: Obs ved mye tubelekkasje! Tidalvolum måles på ekspirasjonsside og ved mye lekkasje vil det kunne gi hypokapni. Ved urolig pasient, mye slim og/eller pasienten presser mot, vil man kunne oppleve at maskinen stadig jobber seg opp i maks amplityde i kortere eller lengre perioder og det blir et mer uklart bilde ventilasjonsmessig. Slå av VG i disse situasjonene. Obs husk å redusere maks amplityde, styr etter pCO2. Husk å kalibrere flow sensor 1x/døgn.
- Pneumothoraks: Vær spesielt oppmerksom på at en pneumothoraks kan arte seg annerledes ved HFV. Pga den meget effektive CO2-utluftningen får man ofte ikke så plutselig og rask stigning som under konvensjonell behandling. Videre er auskultasjon verdiløs ved HFV. Fiberlys (kald rødt lyskilde) er spesielt nyttig i en slik situasjon. Ved usikkerhet ta rtg thorax (eller UL lunger om kompetanse), men kun dersom barnet ikke fremstår som kritisk dårlig. Da må man prioritere drenasje/torakocentese.
- Suging. Små slimmengder i tuben kan få store utslag pga reduksjon av oscillasjonene. Mindre risting og stigende CO2 og fallende amplitude er kliniske tegn og indiserer suging (obs hyper-inflasjon kan gi samme bilde). Bruk kortest mulig tid på sugingen. Unngå suging hvis det ikke er klar indikasjon.
- Frakobling: Dette skal unngås unntatt for helt nødvendige prosedyrer. Årsaken er at en raskt vil få et sammenfall av alveolene og forverring i tilstanden. Max frakoplingstid er 30 sekunder. Ved behov for å auskultere pasienten (duktus) kan en enten klemme av tuben i opptil 5 sekunder, eller slå av oscillasjonene, men holde pasienten tilkoblet (altså på tube-CPAP). Dersom pasienten blir dårligere etter frakopling øker en MAP noen minutter for å rekruttere kollaberte lungeavsnitt. Dette er sterkt å foretrekke framfor bagging/øke FiO2.
- Sjekk fukter slik at denne fungerer adekvat.
- Vann i slangene. Et generelt problem ved HFV og kan påvirke effekten av oscillasjonene. En skal derfor ha fall på slangene (fra pasienten) og følge godt med og få tømt slangene raskt ved synlig fukt.
- Surfactant. Settes gjennom lukket system uten å kople fra. Ofte må amplituden ev. også MAP kortvarig økes (plugging) for deretter å senkes, avhengig av effekten.
- Sedasjon: Ofte ikke nødvendig. Endel egenrespirasjon kan være en fordel for slim mobilisering. Ved åpenbart ubehag, mye uro og/eller egenrespirasjon som interferer sterkt med oscilleringen bør barnet sederes eller i uttalte tilfeller relakseres. Se kapittel om smerte og sedasjon for dosering av medikamenter.
Referanser
- Slutsky AS, et al. Ventilation with Small Tidal Volumes. NEJM 2002; 347:630-1.
- Johnson AH, et al. High-Frequency Oscillatory Ventilation for the Prevention of Chronic Lung Disease of Prematurity NEJM 2002; 347: 633-42.
- Courtney SE, et al. High-Frequency Oscillatory Ventilation versus Conventional Mechanical Ventilation for Very-Low Birth-Weight Infants. NEJM 2002;3 47:643-52.
- Henderson-Smart DJ, et al. High frequency oscillatory ventilation versus conventional ventilation for infants with severe pulmonary dysfunction born at or near term. Cochrane Database of Systematic Reviews 2009, Issue 3.
- Morgan C, et al. Effect of changes in oscillatory amplitude on PaCO2 and PaO2 during high frequency oscillatory ventilation Arch Dis Child Fetal Neonatal Ed. 2000; 82: F237-F242.
- Iscan B, et al. Impact of volume guarantee on high-frequency oscillatory ventilation in preterm infants: a randomized crossover clinical trial. Neonatology 2015; 108: 277–82
- Cools F, et al. Elective high frequency oscillatory ventilation versus conventional ventilation for acute pulmonary dysfunction in preterm infants. Cochrane Database of Systematic Reviews 2015, Issue 3. Art. No.: CD000104.
- Jubal J, et al. Dräger VN500's oscillatory performance has a frequency-dependent threshold. J Paediatr Child Health 2014:50:27-31
- Pillow J. Dräger VN500 HFOV-manual 2016 (meget nyttig lite hefte).
- Sanchez-Luna M, et al. Effect of the I/E ratio on CO2 removal during high-frequency oscillatory ventilation with volume guarantee in a neonatal animal model of RDS. Eur J Pediatr 2016; 175:1343–51
- De Jaegere AP, et al. Individualized lung recruitment during high-frequency ventilation in preterm infants is not associated with lung hyperinflation and air leaks. Eur J Pediatr 2016; 175: 1085–90.
- Gonzalo SG, Target volume-guarantee in high-frequency oscillatory ventilation for preterm respiratory distress syndrome: Low volumes and high frequencies lead to adequate ventilation. Pediatr Pulmonol. 2021:6: 2597-2603
- Belteki G, et al. High-frequency oscillatory ventilation with volume guarantee: a single-centre experience. Arch Dis Child Fetal Neonatal Ed 2019; 104: 384–9
- Tingay DG, et al. Time to Lung Volume Stability After Pressure Change During High-Frequency Oscillatory Ventilation. Critical Care Explorations. 2021; 3(6).
- Ackerman BW, et al. High-frequency ventilation in preterm infants and neonates. Pediatric Research; 2022; Feb 8. doi: 10.1038/s41390-021-01639-8.
- Tana M, et al. Effects of High-Frequency Oscillatory Ventilation With Volume Guarantee During Surfactant Treatment in Extremely Low Gestational Age Newborns With Respiratory Distress Syndrome: An Observational Study. Front Pediatr 2022 March










